Contoh Soal Fraksi Mol Dan Pembahasannya
Contoh Soal Fraksi Mol Beserta Kunci Jawaban. Setelah anda mempelajari latihan soal fraksi mol, anda dapat dengan mudah menyelesaikan bentuk lain dari soal-soal yang berhubungan dengan fraksi mol. Seperti yang kita ketahui dalam menyatakan konstrasi larutan, kita dapat menyatakannya dalam : 1. Fraksi Mol. 2.

FRAKSI MOL X YouTube
Fraksi mol j adalah x j dan seterusnya. Jumlah fraksi mol dari semua komponen larutan adalah 1. Total fraksi mol = x i + x j = 1. Perhatikanlah contoh soal penggunaan fraksi mol berikut. Contoh Soal 1. Larutan glukosa dibuat dengan melarutkan 18 g glukosa (M r = 180 g/mol) ke dalam 250 g air. Hitunglah fraksi mol glukosa.
Sifat Koligatif Larutan (Molalitas, Fraksi Mol, Penurunan Tekanan Uap, Titik Didih, Titik Beku
Dilansir dari Thought Co, fraksi mol tidak memiliki satuan karena merupakan rasio perbandingan. Rumus fraksi mol. Rumus fraksi mol adalah jumlah mol zat yang dicari fraksi molnya, dibagi dengan jumlah mol zat dalam campuran. Fraksi mol dilambangkan dalam huruf "chi" Yunani, yaitu "x". Rumus fraksi mol zat terlarut

Menghitung Fraksi Mol YouTube
Dalam ilmu kimia, fraksi mol menunjukkan perbandingan mol suatu zat dengan mol total semua zat dalam larutan. Fraksi mol terbagi menjadi dua macam, yaitu fraksi mol zat terlarut (Xt) dan fraksi mol zat pelarut (Xp). Dikutip dari Sifat Koligatif Larutan oleh Haqqi Annazili Nasution, dkk. (2022: 3.

Kimia 12 Molaritas Molalitas dan Fraksi Mol YouTube
Fraksi mol adalah perbandingan jumlah mol zat X dengan mol total yang ada dalam larutan. Fraksi mol dirumuskan sebagai berikut: X t + X p = 1. Keterangan; Xt = fraksi mol zat terlarut. Xp = fraksi mol zat pelarut. nt = mol zat terlarut. np = mol zat pelarut. Perhatikan contoh soal fraksi mol berikut ini: Sebanyak 7,1 gram Na 2 SO 4 (Mr = 142.

Contoh Soal Fraksi Mol Dan Pembahasannya
Blog KoKim - Fraksi mol (X) merupakan satuan konsentrasi yang menyatakan perbandingan antara jumlah mol salah satu komponen larutan (jumlah mol zat pelarut atau jumlah mol zat terlarut) dengan jumlah mol total larutan. Fraksi mol disimbolkan dengan X . Misal dalam larutan hanya mengandung 2 komponen, yaitu zat B sebagai zat terlarut dan A sebagai pelarut, maka fraksi mol A disimbolkan X$_A.
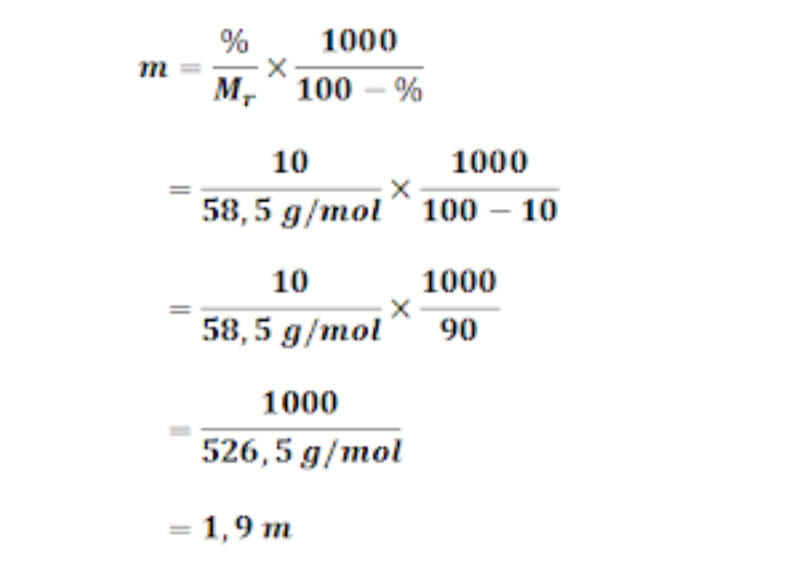
Cara Menghitung dan Contoh Soal Fraksi Mol dan Jawabannya Rumus dan Pembahasan Fraksi Mol
Agar lebih memahami tentang pengertian dan rumus fraksi mol, maka sebaiknya berlatih soal adalah hal yang paling ampuh, dibawah ini contoh - contoh soal fraksi mol lengkap dengan pembahasannya. Contoh Soal 1. Sebuah larutan terdiri dari 3 mol zat A, 3 mol zat B, dan 4 mol zat C. Hitung fraksi mol dari masing - masing zat tersebut ? Pembahasan :

Contoh Soal Fraksi Mol
Fraksi mol banyak digunakan dalam diagram fasa. Propertinya antara lain: tidak tergantung temperatur (berbeda dengan konsentrasi molar) dan tidak membutuhkan data densitas fasa. dijumlahkan nilainya satu: jika x1=0.1 maka x2=0.9, salah satunya menjadi solvent dan yang lainnya solute. Pada campuran gas ideal, fraksi mol dapat dinyatakan sebagai.

Kumpulan Contoh Soal Fraksi Mol dan Pembahasannya Terbaru 2022 Halaman 4
Fraksi Mol Zat Pelarut (X P); Selanjutnya ada rumus untuk mencari fraksi mol dari zat pelarut. Caranya mirip banget dengan yang tadi. Elo cukup memasukkan jumlah dari mol zat pelarut (n p), kemudian elo bagi dengan jumlah dari mol keseluruhan alias mol zat terlarut (n t) ditambah dengan mol zat pelarut (n p).. Biar lebih jelas, gue juga udah buat ilustrasinya di bawah ini.

Foto Fraksi Mol Pengertian dan Rumusnya
Contoh perhitungan fraksi mol. Misalkan suatu larutan yang dibuat dari 5,85 gram garam dapur (Mr = 58,5) yang dilarutkan dalam 90 gram air (Mr = 18). Maka fraksi mol garam dapur dan fraksi mol air bisa dihitung dengan cara : Mol garam dapur, nG = 5,85/58,5 =0,1 mol

Contoh soal Fraksi mol dan penyelesaiannya .. YouTube
Fraksi Mol dalam Kimia Fraksi mol adalah ukuran konsentrasi larutan yang menyatakan perbandingan jumlah mol sebagian zat terhadap jumlah mol total komponen larutan. Dalam kimia, fraksi mol didefinisikan sebagai jumlah konstituen dibagi dengan jumlah total semua konstituen dalam suatu campuran : Jumlah semua fraksi mol sama dengan 1: Fraksi mol juga disebut fraksi jumlah dan identik dengan.

Kumpulan Soal Fraksi Mol Terlarut Dan Pelarut Lengkap Dengan Pembahasan Riset
Jadi, fraksi mol masing - masing adalah : X A = 0,25. X B = 0,5. X C = 0,25. Dari ketiga fraksi mol di atas, jika dijumlahkan harus menghasilkan 1 sesuai rumus : X A + X B + X C = 1. 0,25 + 0,5 + 0,25 = 1. Demikian pembahasan dari kami, semoga bermanfaat dan menambah wawasan serta pengetahuan kalian. Sekian terima kasih.

Contoh Soal Fraksi Mol Dan Pembahasannya
mole fraction. In chemistry, the mole fraction or molar fraction, also called mole proportion or molar proportion, is a quantity defined as the ratio between the amount of a constituent substance, ni (expressed in unit of moles, symbol mol), and the total amount of all constituents in a mixture, ntot (also expressed in moles): [1] It is denoted.

MENGHITUNG FRAKSI MOL JIKA DIKETAHUI MOLAL YouTube
Pengertian Fraksi Mol. Fraksi mol adalah besaran konsentrasi larutan. Fraksi mol menyatakan perbandingan jumlah mol zat terlarut terhadap jumlah mol larutan. Fraksi mol tidak memiliki satuan, sehingga dinotasikan dengan X. Contohnya fraksi mol urea 01, ditulis dengan X urea 0,1. Artinya, larutan yang mengandung 0,1 bagian mol urea dalam 1.

Fraksi mol dan molalitas (m) Soal dan Pembahasan KIMIA KELAS 12 YouTube
Jadi, fraksi mol NaCl dan fraksi mol H 2 O berturut-turut adalah 0,231 dan 0,769. FYI, hasil penjumlahan antara fraksi mol pelarut dan zat terlarut itu sama dengan satu, ya. Secara matematis bisa ditulis x pel + x ter = 1.

KIMIA KELAS XII Fraksi Mol Pelarut & Fraksi Mol terlarut. YouTube
Dilansir ByJu's, fraksi mol merupakan satuan konsentrasi.Dalam sebuah larutan, jumlah relatif zat pelarut dan terlarut diukur menggunakan fraksi mol dan disimbolkan sebagai 'X'. Dalam pengukuran, fraksi mol didapat dari jumlah mol komponen tertentu dalam pelarut dibagi dengan jumlah total mol terlarut.