
Materi Kimia Elektrolit dan Non Elektrolit YouTube
KOMPAS.com - Berdasarkan kemampuannya menghantarkan listrik, larutan kimiawi terbagi menjadi dua, yaitu elektrolit dan nonelektrolit. Larutan elektrolit sangat penting dalam tubuh manusia. Kekurangan elektrolit akibat keringat berlebih yang parah bisa membahayakan jiwa. Kekurangan elektrolit dalam tubuh bisa membuat otot menjadi lemah dan detak jantung tinggi yang bisa memicu serangan jantung.

30 Contoh Larutan Elektrolit dan Non Elektrolit
Apa Itu Larutan Elektrolit dan Non-elektrolit? Larutan elektrolit dan non-elektrolit adalah istilah yang sering digunakan dalam kimia untuk menggambarkan sifat-sifat larutan berdasarkan kemampuan mereka untuk menghantarkan arus listrik. Dalam hal ini, elektrolit merujuk pada zat yang dapat memecah menjadi ion-ion saat larut dalam air dan.

LARUTAN ELEKTROLIT DAN NONELEKTROLIT ( KIMIA SMA KELAS 10 ) YouTube
Lalu apa yang dimaksud dengan larutan elektrolit dan non elektrolit? Kamu bisa lihat gambar percobaan daya hantar listrik dari beberapa larutan di bawah ini. Gambar di atas merupakan hasil pengujian daya hantar listrik terhadap beberapa larutan: Gelas A : Larutan nonelektrolit. Gelas B: Larutan elektrolit lemah. Gelas C : Larutan elektrolit kuat

Mengenal Larutan Elektrolit dan Non Elektrolit Kimia Kelas 10
Artinya, larutan non elektrolit tidak mengandung ion-ion (kation atau anion) yang dapat menghantarkan muatan listrik. Dilansir dari Chemistry LibreTexts, hal tersebut karena zat non elektrolit tidak berdisosiasi sama sekali dan rumus kimia zat tersebut tidak berubah selama proses pelarutan. Zat elektrolit cenderung memiliki ikatan kovalen yang.

Larutan Elektrolit dan Non Elektrolit
Contoh dari larutan non-elektrolit adalah CO(HN2)2, CH3OH, C6H12)6, dan C2H5OH. Jenis-Jenis Larutan Elektrolit.. Oleh karena itu, padatan senyawa ionik tidak dapat menghantarkan listrik. Jika padatan tersebut dilelehkan atau dilarutkan dalam air, maka ion-ion tersebut dapat terurai dari kisinya dan bergerak bebas sehingga dapat menghantarkan.

Larutan Elektrolit dan Non Elektrolit, Ini Contoh dan Perbedaannya!
Larutan elektrolit dapat menghantarkan arus listrik karena adanya ion-ion yang terbentuk, sedangkan larutan non-elektrolit tidak dapat menghantarkan arus listrik. Selain itu, larutan elektrolit dapat mengalami disosiasi, sementara larutan non-elektrolit tidak. Larutan elektrolit juga cenderung memiliki konduktivitas yang lebih tinggi.
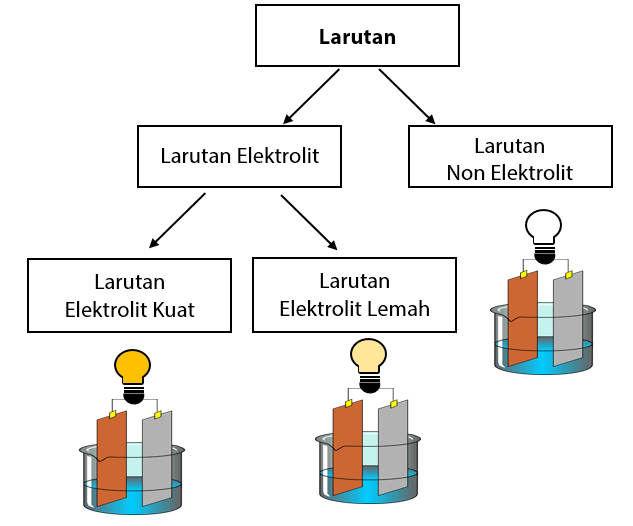
Larutan Elektrolit dan Non Elektrolit
Ciri-ciri dari larutan non-elektrolit: Pada larutan non elektrolit, senyawa dalam air tidak mengalami proses ionisasi. Larutan non-elektrolit tidak dapat terionisasi dalam air, maka 𝛼 = 0. Larutan non-elektrolit terdiri atas kelompok senyawa organik molekular yang larut. Tidak menghantarkan arus listrik; Contoh larutan non-elektrolit.
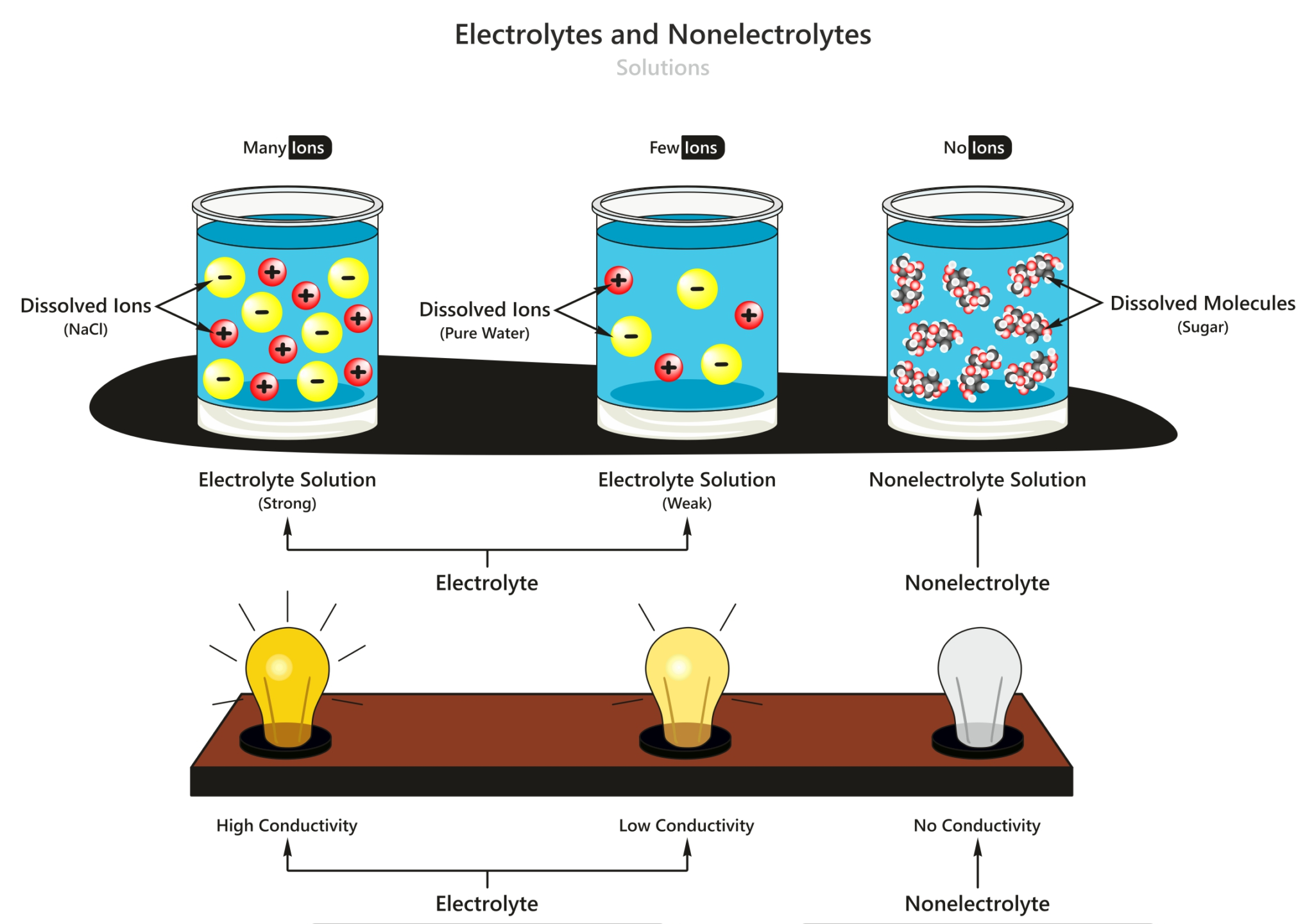
Materi Larutan Elektrolit Dan Non Elektrolit Homecare24
Apa Itu Larutan Berair? Pengertian Kimia dan Contohnya. 11 Sep, 2019. Perbedaan Elektrolit Kuat dan Elektrolit Lemah. 06 Aug, 2019. Apa Itu Senyawa Ionik dan Kovalen? 29 Jun, 2018.. Apa Itu Elektrolit Lemah? 19 Jul, 2019. Memahami Apa Arti Kelarutan dalam Kimia. 22 Jan, 2020. Apa Itu Asam Lemah?

Larutan Elektrolit dan Non Elektrolit (Kompone
Larutan Elektrolit dan Non-Elektrolit: Sejarah Penemuan Larutan Elektrolit dan Non-Elektrolit. Penemuan larutan elektrolit dan non-elektrolit ternyata berhubungan dengan ilmuwan asal Swedia, Svante August Arrhenius (1859-1927). Kala itu ia tengah melakukan presentasi disertasi untuk gelar PhD-nya di Universitas Uppsala tahun 1884.
30 Soal Kimia BAB Larutan ElektrolitNon Elektrolit
Jika dibandingkan, larutan elektrolit dan larutan non-elektrolit dengan konsentrasi yang sama akan memiliki jumlah partikel yang berbeda. Jumlah partikel larutan elektrolit lebih banyak daripada larutan non-elektrolit sehingga sifat koligatifnya pun akan lebih besar. ΔP = P⁰.

Larutan Elektrolit dan Non Elektrolit (Kimia SBMPTN, UN, SMA) YouTube
Larutan elektrolit tinggi memiliki derajat ionisasi (α) yang mendekati 1, berarti zat terlarut hampi semuanya terionisasi. Adapun larutan elektrolit lemah memiliki derajat ionisasi jauh dibawah 1, berarti zat terlarut yang berubah menjadi ion hanya sedikit. Hal ini menyebabkan larutan elektrolit lemah menghantarkan listrik dengan kurang baik.
Contoh Larutan Elektrolit Dan Non Elektrolit Lengkap Berbagai Contoh
Pada akhirnya, ketiadaan proses itu menyebabkan arus listrik tidak bisa mengalir di larutan non elektrolit. Contoh larutan non elektrolit adalah alkohol (yang memiliki kandungan sebesar 70%), larutan urea, larutan gula, larutan glukosa, dan beberapa larutan lainnya. Berikut ini daftar perbedaan antara larutan elektrolit dan non elektrolit.

Larutan Elektrolit dan Non Elektrolit. Materi Kimia SMA/MA Kelas X
Larutan seperti ini disebut larutan elektrolit. Sebaliknya, larutan yang tidak bisa menghantarkan arus listrik disebut larutan non elektrolit. Keduanya memiliki manfaat yang sangat penting dalam kehidupan manusia, bahkan larutan elektrolit dibutuhkan tubuh agar organ tubuh, seperti otak, saraf, dan otot dapat berfungsi dengan baik.

Larutan Elektrolit dan Nonelektrolit
Larutan dibagi menjadi dua, yaitu larutan elektrolit dan non elektrolit yang mana masing-masing mempunyai karakteristik sendiri. Yuk, simak di sini!. kamu harus mengetahui terlebih dahulu apa itu larutan. Jadi, larutan bukan berarti air ya, tapi larutan adalah suatu campuran homogen yang terdiri dari dua atau lebih zat. Dimana, zat yang.

Elektrolit Kuat dan Elektrolit Lemah (Kimia SBMPTN, UN, SMA) YouTube
Di sisi lain, non-elektrolit adalah zat yang tidak dapat terionisasi dan tidak dapat membentuk ion-ion di dalam larutan. Karena itu, non-elektrolit tidak dapat menghantarkan arus listrik. Cara Kerja Elektrolit dan Non-Elektrolit. Ketika elektrolit larut dalam air atau berada dalam larutan, molekul zat tersebut terurai menjadi ion-ion.

Memahami Larutan Elektrolit dan Nonelektrolit beserta Contohnya Kimia Kelas 10
Sedangkan untuk larutan non elektrolit bisa kamu temukan ketika kamu mengkonsumsi gula dalam minuman. Gula merupakan contoh larutan non-elektrolit. Saat kamu mencampurkan gula ke dalam air, gula tidak terurai menjadi ion-ion seperti pada larutan elektrolit. Itu sebabnya larutan gula tidak menghantarkan listrik.